近年来,我国超重和肥胖人群的患病率呈持续上升趋势。作为慢性疾病中的独立病种及多种慢性疾病的重要致病因素,肥胖症已成为我国重大公共卫生问题,是我国第六大致死致残主要危险因素。为规范我国肥胖症临床诊疗,为患者提供个性化诊疗方案,并不断提高医疗机构肥胖症诊疗同质化水平,提升肥胖症治疗效果,改善长期预后,国家卫生健康委制定了本指南。现丁香园对其主要内容进行整理,以供参考。
1
肥胖症的定义
世界卫生组织(World Health Organization,WHO)将肥胖症定义为对健康产生不良影响的异常或者过度脂肪蓄积。
通常,脂肪组织并非在全身均匀分布,腹腔内脏脂肪和皮下脂肪比例存在个体间差异,故呈现出对人体代谢影响的不同表现特征。
近年来,也有一些学术组织和学者建议以「以肥胖为基础的慢性疾病」(adiposity-based chronic disease,ABCD)来定义肥胖症。
2
肥胖症的病因
1. 遗传因素
遗传因素在肥胖症的发生发展中具有重要作用。流行病学调查表明,肥胖症具有家族聚集性,提示肥胖症可能与家族中的遗传背景相关。人类遗传学研究结果显示,与肥胖易感性相关的遗传基因可能涉及能量代谢、食欲调控、脂肪细胞分化等多个方面。一些罕见的遗传病,如 Prader-Willi 综合征(Prader-Willi Syndrome,PWs)和家族性瘦素受体(leptin receptor,LEPR)基因突变等,亦可导致肥胖症的发生。
2. 生活方式因素
(1)饮食
过多摄入高能量、高脂肪、高糖、低膳食纤维的食物和饮料,通过刺激神经中枢摄食神经元,引发进食过量、进食行为不规律等不良饮食习惯可导致肥胖症。
此外,长期高油、高糖膳食会破坏能量摄入消耗和脂肪合成分解平衡。
保持营养均衡的饮食,合理摄入蛋白质、脂肪、碳水化合物、维生素和矿物质等营养素,有助于降低肥胖症发生风险。
(2)身体活动
缺乏身体活动是导致肥胖症的重要原因。身体活动可以消耗能量,有助于控制体重。
此外,身体活动产生的一系列代谢有益分子对抑制进食和增强人体能量消耗有额外益处。
身体活动亦可增加肌肉力量和肌肉含量,减少脂肪堆积,增强胰岛素受体敏感性。
(3)精神心理
精神压力会影响人体下丘脑-垂体-肾上腺轴,促进皮质醇释放,引起食欲上升和进食行为改变。
精神压力还可能影响胰岛素的分泌和外周组织受体功能变化,胰岛素不适当分泌和外周组织胰岛素抵抗的共同作用促进肥胖症的发生。
此外,暴食、亚健康的压力性进食以及精神科药物也可导致肥胖症。
(4)睡眠习惯
不良的睡眠习惯也是肥胖症的重要危险因素。
睡眠时间不足可导致胃饥饿素、瘦素和肽 YY(Peptide YY,PYY)分泌失衡从而引起进食增多和能量消耗减少。
而睡眠时间过长使机体处于低能耗状态,能量转化为脂肪储存于体内,引发生理失调性肥胖。
3. 疾病和药物因素
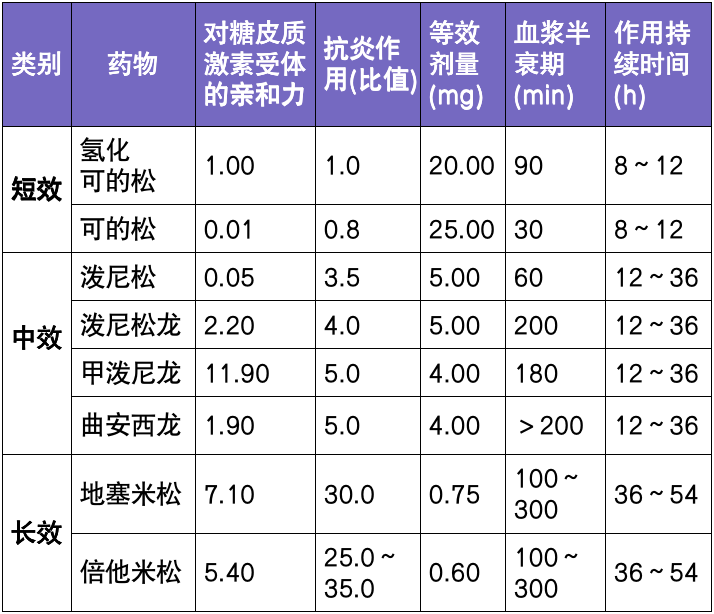
一些疾病如库欣综合征等,以及一些药物,如类固醇药物中的泼尼松和氢化可的松,和抗抑郁药物中的米氮平、曲唑酮、度洛西汀和阿米替林等,均可导致体重增加,引发肥胖症。
此外,肠道菌群失调也与肥胖症及其代谢紊乱发生的风险增加相关。
4. 环境和社会因素
经济快速发展、城市化进程加速、粮食供给模式改变、环境污染、以久坐为主的工作方式、拥挤的生活环境等均可促使公众的生活方式发生改变,进而导致易感个体出现超重和肥胖症。
社会因素如经济状况、文化背景、社会时尚、社会规范、社会舆论、政策导向等也会对公众的体重产生潜移默化的影响。
3
肥胖症的诊断标准
1. 基于体质指数的诊断标准
体质指数(body mass index,BMI,kg/m2)是评估全身性肥胖的通用标准,该指数应用身高对体重进行校正,以减少身高因素对肥胖症评估的影响,其计算方式为:体重(kg)除以身高(m)的平方。
研究显示,一般人群 BMI 与体脂比具有良好的相关性,并可反映肥胖症相关疾病的患病风险。
我国成年人群的标准:
低体重状态:BMI < 18.5 kg/m2
正常体重:18.5 kg/m2 ≤ BMI < 24 kg/m2
超重:24 kg/m2 ≤ BMI < 28 kg/m2
肥胖症:BMI ≥ 28 kg/m2
为指导临床诊疗,需要对肥胖症的程度进一步分级根据肥胖症国际分级标准及亚洲人群特征,以及本指南专家组的讨论共识,建议:
轻度肥胖症:28.0kg/m2 ≤ BMI < 32.5kg/m2
中度肥胖症:32.5kg/m2 ≤ BMI < 37.5 kg/m2
重度肥胖症:37.5kg/m2 ≤ BMI < 50 kg/m2
极重度肥胖症:BMI ≥ 50 kg/m2
然而,应用 BMI 作为肥胖症评估指标,存在一定的局限性。随着年龄增长,瘦体重(去脂体重)逐渐降低,体脂含量逐渐上升,因而具有相同 BMI 的青年人和老年人,体脂比会存在差异;在相同 BMI 水平下,经常从事高强度体力活动者和专业运动员的体脂比通常低于一般人群。
2. 基于体型特征的诊断标准
脂肪组织在人体内的分布存在异质性,我国人群以腹腔内脏脂肪分布较多为主要特征,故较易形成中心性肥胖(腹型肥胖)。
腰围是反映中心性肥胖的常用指标,基于我国成年人群特点和健康风险评估,正常腰围定义为 < 85 cm(男性)和 < 80 cm(女性),腰围 > 90 cm(男性)和 > 85 cm(女性)即可诊断为中心性肥胖。
此外,腰围/臀围比(waist-hip ratio,WHR)是另一个反映中心性肥胖的指标,当 WHR > 0.90(男性)和 > 0.85(女性)时,也可诊断为中心性肥胖。
需要注意的是,腰围和 WHR 随着年龄增长呈缓慢增长趋势。
3. 基于体脂比的诊断标准
体脂比是指人体内脂肪重量在人体总体重中所占的比例,又称体脂百分数,以反映人体内脂肪含量的多少。
常采用的测量方法包括:皮褶厚度测量、生物电阻抗分析(bioelectrical impedance analysis,BIA)和双能 X 射线吸收测定法(dual energy X-ray absorptiometry,DEXA)、用于测量体内脂肪的计算机断层扫描(computer tomography,CT)和磁共振成像(magnetic resonance imaging,MRI)等。
目前将成年人体脂比超过 25%(男性)或者 30%(女性)定义为体脂过多,但其局限性在于较难全面反映体内脂肪组织的分布,不是常规的临床诊断方法。
4. 儿童青少年肥胖症的诊断标准
根据有关行业标准,对于 7 岁以下儿童,可以性别年龄别 BMI 的标准差作为评价方法;对于 6~18 岁学龄儿童青少年,可以性别年龄别 BMI 作为筛查超重与肥胖标准,并与中国成人超重、肥胖筛查标准接轨。
4
肥胖症的检查评估
1. 体格检查项目
(1)人体测量学指标及相关指标计算:身高、体重、腰围臀围、BMI、腰臀比。
(2)肥胖症相关疾病或导致继发性肥胖症的疾病相关体征:如黑棘皮、满月脸、水牛背、腹部宽大紫纹、甲状腺肿等。
2. 实验室检查项目
(1)肥胖症相关疾病评估,需至少包括:
① 血糖、糖化血红蛋白、胰岛素水平;
② 血脂谱:TC、HDL-C、LDL-C、TG;
③ 血尿酸;
④ 肝功能:谷丙转氨酶、谷草转氨酶直接胆红素、间接胆红素;
⑤ 肾功能:血肌酐、肾小球滤过率(estimated glomerular filtration rate,eGFR)等。
(2)评估有无导致肥胖症的继发性原因,需至少包括:
① 甲状腺功能:促甲状腺激素(thyroid stimulating hormone,TSH)及游离 T4 水平(free thyroxine,FT4);
② 库欣综合征筛查:当临床疑似存在库欣综合征时进行筛查;
③ 性腺功能:当临床疑似存在性腺功能减退时进行筛查。
3. 体脂含量及内脏脂肪含量测定
(1)体脂含量测定
体脂含量是指体内脂肪的含量或脂肪占总体重的百分比,目前测定脂肪含量的方法有 BIA、DEXA、皮褶厚度法等。
BIA 法可作为临床初步筛查应用,如需进一步精确评估,可使用 DEXA 法,可以较为准确地评估脂肪、肌肉、骨骼的含量及分布。
(2)内脏脂肪含量测定
内脏脂肪含量测定可反映内脏脂肪聚积程度,常用的方法有腹部 CT 和 MRI,二者均可较为精准地反映脂肪在内脏及外周组织的分布,但上述影像学检查多用于研究,通常不作为临床常规检查项目。
(3)肥胖症相关疾病评估
肥胖症相关疾病初筛可以问卷方式进行,常用问卷包括健康状况调查问卷(36-item short-form、摩尔海德生活质量问卷)、体重对生活质量影响量表(the impact ofweight on quality of life,IWQOL-Lite)、抑郁自评量表(self-rating depression scale,SDS)、焦虑自评量表(self-rating anxiety scale,SAS)、Epworth 嗜睡程度评价表、睡眠呼吸暂停初筛量表(STOP-Bang questionnaire,STOP-BANG)、胃食管反流自测量表(gastroesophagealreflux disease questionnaire,GERD-Q)等。
对于 OSAS,可应用便携式睡眠监测记录仪进行评估,必要时可行多导睡眠监测(polysomnography,PsG)。
对于 NAFLD,可行腹部(肝脏)超声、肝脏瞬时弹性成像、腹部(肝脏)CT 或 MRI 检查,采用肝纤维化 4 因子指数(fibrosis 4 score,FIB-4)、NAFLD 肝纤维化评分(NAFLD fibrosis score,NFS),必要时通过肝脏活检病理进一步评估肝脏疾病进展。
其他导致肥胖症的继发性病因筛查,包括但不限于:
①甲状腺:临床疑似甲状腺相关疾病时可进行甲状腺超声检查;
②肾上腺:临床疑似肾上腺相关疾病时可进行肾上腺 CT 或超声检查;
③脑垂体:临床疑似垂体相关疾病时可进行垂体 MRI 检查。
4. 功能学检查
流行病学研究显示,超重或肥胖症与生活质量下降以及心血管疾病发生风险增加密切相关,因此有必要对肥胖症患者进行身体功能评估,了解体重对于其生活的影响,必要时还需要对重要脏器功能进行评估,包括如超声心动图、心肺运动功能评估、运动能力评估、基础代谢分析等相关检查。
5. 其他评估内容
为了充分了解肥胖症患者的病因,并制定最合理的个体化诊疗方案,还需要对患者进行家庭、社会资源支持评估,并了解患者减重的动机以及预期目标,与患者共同商讨合理的减重计划。
5
肥胖症的治疗流程
肥胖症治疗的主要目的在于减少蓄积在体内过多的脂肪,降低肥胖症相关疾病的发生风险,缓解或改善已合并的肥胖症相关疾病和精神心理异常,提高肥胖症患者的健康水平和社会适应能力。此外,改善与肥胖相关的精神心理障碍和症状、提高肥胖症患者的社会适应水平也是肥胖症治疗的重要内容。
肥胖症的减重目标应进行分层设定,需综合考虑肥胖症的程度以及肥胖症相关疾病的风险和程度。
对于大多数超重和轻度肥胖症患者,可设定为在 3~6 个月之内至少将体重降低 5%~15% 并维持;对于中、重度肥胖症患者则可设定更高的减重目标,以获得代谢异常和相关临床结局的更优改善。
同时,减重的速率也需要关注,减重速率与肥胖症程度和所采取的减重方式相关,减重过程中需关注脱水、肌少症和内分泌系统的变化,建议每 3~6 个月对减重效果和代谢指标进行评估。
肥胖症治疗有多种手段,主要包括:行为心理干预、运动干预、临床营养治疗、药物治疗、外科手术治疗以及中医药治疗等。
此外,近年来数字健康工具,如可穿戴设备、移动健康应用程序、远程监测设备等在肥胖症管理中得到研究和应用。
在制定减重治疗方案时,应充分考虑患者心理预期,通过医患共同决策,综合使用不同手段,以期获得最佳治疗效果。
一般建议所有患者均应接受营养、运动、心理指导作为全程基础管理。
根据超重和肥胖症程度、肥胖症相关疾病风险和程度,在基础治疗之上,本指南推荐采取如下诊疗路径(图 1)。
图 1 超重和肥胖症诊疗路径
6
运动干预
主动运动是肥胖症运动干预的重要措施。
对于肥胖症患者,运动干预方案应以注重患者安全为原则,在运动风险评估(包括机械性损伤风险和运动诱发疾病风险)的基础上,根据患者的 BMI、体能、基础疾病和肥胖症相关疾病制定个体化运动处方,包括运动频率、强度、方式、时间、总量以及减重过程中的运动进阶,随访运动执行情况,并进行动态评估,适时根据心肺功能和健康状况的改善逐渐增加运动总量和强度。
7
临床营养治疗
临床营养治疗(medicalnutrition therapy,MNT)是肥胖症综合治疗的基础疗法,指在临床条件下对肥胖症采取特殊营养干预措施的总称,包括个体化营养筛查、营养状况评定、营养诊断、制定营养干预计划,并在一定时期内实施与监测。
肥胖症临床营养治疗可分四步,即营养筛查及评估、干预、监测、营养教育与管理。
医学减重膳食是为了满足肥胖症患者的基本能量需求和减重需求而采取的调整营养素比例的膳食方式,主要包括限能量饮食、高蛋白饮食、轻断食模式、低碳水化合物饮食等方式(见表 1)。
表 1 常用医学减重膳食方法的临床应用
医学减重膳食应注意,一种膳食方案并非适于所有肥胖症患者,应根据代谢状态和身体状况在临床营养(医)师指导和临床监测下进行,目前尚无研究证据表明其长期的健康效益。
8
药物治疗
近些年来,减重药物的研发进展迅速,尤其是以胰高血糖素样肽-1 受体激动剂(glucagon-like peptide-1 receptolagonist,GLP-1 RA)为基础的新型减重药物不断问世,减重效果也不断提升。
目前在我国共有五种药物获得国家药品监督管理局批准用于成年原发性肥胖症患者减重治疗,包括奥利司他、利拉鲁肽、贝那鲁肽、司美格鲁肽及替尔泊肽。我国目前尚未批准用于治疗遗传性肥胖症的药物。
需要注意的是,应用药物治疗肥胖症应该严格把握适应证,规范使用,需要在充分评估患者病情及有无禁忌证后方可起始应用,同时在使用药物减重的过程中也需要定期在专业医师指导下进行规律随访,监测药物的有效性及安全性,根据情况适时调整治疗方案。
1. 减重药物的适应证
当超重且伴有至少一种体重相关合并症,如高血糖、高血压、血脂异常、脂肪肝、阻塞性睡眠呼吸暂停综合征、心血管疾病等通过生活方式干预无法达到减重目标时,可在生活方式干预的基础上联合应用减重药物治疗。肥胖症通过生活方式干预无法达到减重目标时,可在生活方式干预的基础上联合应用减重药物治疗。
2. 减重药物及其应用
目前在我国有五种减重药物获得国家药品监督管理局批准用于成年原发性肥胖症患者减重,具体详见表 2。
表 2 国内已获批用于治疗原发性肥胖症的药物
(1)奥利司他
奥利司他是一种脂肪酶抑制剂,通过抑制胃肠道的脂肪酶,减少肠腔黏膜对膳食中甘油三酯的吸收,促进脂肪从肠道排出体外,在我国被批准用于超重或肥胖症患者的减重治疗。
用法用量:该药建议餐时或餐后一小时内口服,每日三次,每次推荐口服剂量 120 mg。
禁忌:用于吸收不良综合征、胆汁淤积症、继发性肥胖的患者,由于奥利司他会干扰抗移植排斥反应的药物,器官移植者以及服用环孢霉素患者禁用。
副作用:主要为胃肠道反应,包括脂肪泻、大便次数增多、胃肠排气增多等。
注意事项:长期使用需注意监测药物相关副作用。
研究疗效:临床试验显示持续应用奥利司他,去除安慰剂效应后的体重下降幅度约为 3.1%,减重幅度达到 5% 以上的患者比例为 49.7%。在长达四年的时间中,去除安慰剂效应后减重幅度仍可达 2.8%。
(2)利拉鲁肽
利拉鲁肽为 GLP-1 RA 的长效制剂。该药物作用于下丘脑,增加饱食信号,减少饥饿信号;同时作用于胃肠道,延缓胃排空,减少胃酸分泌,从而达到通过减少能量摄入使体重降低的效果。
用法用量:该药为一天一次皮下注射,用于成人减重最高剂量为每日 3.0 mg。
禁忌:虽然有研究显示利拉鲁肽在临床相关的药物暴露水平可能导致啮齿类动物甲状腺 C 细胞肿瘤,目前尚无证据表明该药会导致人类甲状腺 C 细胞肿瘤(包括甲状腺髓样癌),但鉴于安全性考虑,利拉鲁肽不得用于有甲状腺髓样癌既往史或家族史的患者以及 2 型多发性内分泌肿瘤综合征患者。
副作用:主要为胃肠道反应,也是治疗期间最常见的不良反应,包括恶心、呕吐、腹泻、便秘、消化不良、腹痛等。
注意事项:如果使用利拉鲁肽 16 周,体重减少无法达到基线体重的 4% 以上,则建议考虑停用利拉鲁肽,因为这类患者即使继续使用,实现具有临床意义的体重减轻的概率也很低。
研究疗效:临床试验显示持续应用利拉鲁肽,去除安慰剂效应后的体重下降幅度约为 4.7%,减重幅度达到 5% 以上的患者比例为 64%。在一项用药 56 周的研究中,去除安慰剂效应后,利拉鲁肽平均减重幅度为 5.4%。
(3)贝那鲁肽
贝那鲁肽为 GLP-1 RA 的短效制剂,通过增加饱腹感、延缓胃排空达到减轻体重的作用。
用法用量:贝那鲁肽用于减重的剂量为每次 0.2 mg,每日三次皮下注射。
禁忌:
对该药所含任何成分过敏者。
该药在非临床研究、以及临床试验过程中尚未发现与甲状腺 C 细胞相关的不良反应,但因其他 GLP-1 类似物有可能导致啮齿类动物甲状腺 C 细胞肿瘤,因此本品同样不得用于有甲状腺髓样癌既往史或家族史患者以及 2 型多发性内分泌肿瘤综合征患者。
副作用:主要为胃肠道反应,其他在研究中观察到的不良反应还包括头晕、头痛、非严重低血糖事件、注射部分反应等。
研究疗效:临床试验显示持续应用贝那鲁肽 12~24 个月时,去除安慰剂效应后的体重下降幅度为 3.6%,减重幅度达到 5% 以上的患者比例为 58.2%。
(4)司美格鲁肽
司美格鲁肽为 GLP-1 RA 的长效制剂,同样通过作用于中枢降低饥饿感,增加饱腹感,降低能量摄入,改善饮食控制实现减重。
用法用量:司美格鲁肽起始剂量为 0.25 mg 每周一次皮下注射,维持剂量为 2.4 mg 或 1.7 mg 每周一次。
禁忌:
研究显示在啮齿类动物中,司美格鲁肽可能引起甲状腺 C 细胞肿瘤,但目前尚无证据表明该药会导致人类甲状腺 C 细胞肿瘤,包括甲状腺髓样癌。出于安全性考虑,司美格鲁肽不得用于有甲状腺髓样癌既往史或家族史患者以及 2 型多发性内分泌肿瘤综合征患者,同时在使用该类药物时,应告知患者可能的甲状腺髓样癌风险及甲状腺肿瘤的症状。
该药品也禁用于对其活性成分或其中任何辅料过敏者。
副作用:最常见的不良反应为胃肠系统疾病,包括恶心、腹泻、便秘、呕吐等。
研究疗效:
在亚洲地区主要包括日本、韩国为主的超重或肥胖人群中进行的研究显示,去除安慰剂效应后,司美格鲁肽 2.4 mg 在 68 周时的减重幅度可达 11.1%,在以中国人为主的超重或肥胖人群中进行的研究显示,去除安慰剂效应后,司美格鲁肽 2.4 mg 在 44 周时的减重幅度可达 8.5%,司美格鲁肽组 85% 的受试者减重幅度达到 5% 或以上。
同时,司美格鲁肽 2.4 mg 还显示具有心血管保护作用,在一项旨在研究司美格鲁肽 2.4 mg 对已确诊心血管疾病的非糖尿病的超重/肥胖成人主要不良心血管事件(major adverse cardiac events,MACE)风险降低的研究中,随访 39.8 月,司美格鲁肽 2.4 mg 每周一次皮下注射可显著降低主要心血管不良事件发生风险达 20%,同时改善多种心血管疾病风险因素。
(5)替尔泊肽
替尔泊肽是针对 GLP-1 受体和葡萄糖依赖性促胰岛素分泌多肽(glucose-dependent insulinotropic polypeptide,GIP)受体的双靶点激动剂,可通过调节食欲来减少食物摄入、降低体重和减少脂肪量。
用法用量:替尔泊肽推荐起始剂量为 2.5 mg,皮下注射,每周一次;最大给药剂量为 15 mg,皮下注射,每周一次。
禁忌:研究显示替尔泊肽可能导致大鼠甲状腺 C 细胞肿瘤,但目前尚无证据表明该药会引起人类甲状腺 C 细胞肿瘤,包括甲状腺髓样癌。出于安全性考虑,应用替尔泊肽时应告知患者关于甲状腺髓样癌的潜在风险和甲状腺肿瘤的症状。并禁止用于具有甲状腺髓样癌的个人病史或家族史,或 2 型多发性内分泌腺瘤综合征患者。以及已知对替尔泊肽或产品中的任何辅料成分存在严重超敏反应者禁用。
副作用:替尔泊肽最常见的不良反应为胃肠道反应,包括恶心、呕吐、腹泻、便秘、腹痛、消化不良等。
研究疗效:临床试验显示持续应用替尔泊肽 10~15 mg 每周一次 12~24 个月时,根据使用剂量不同,去除安慰剂效应后的体重下降幅度为 11.9%~17.8%,减重幅度达到 5% 以上的患者比例为 85%~91%。在中国人群中进行的替尔泊肽减重效果研究中,去除安慰剂效应后,使用 10~15 mg 替尔泊肽的减重幅度可达 11.3%~15.1%,减重幅度达到 5% 以上的患者比例为 85.8%~87.7%。
9
减重与代谢手术治疗
1. 手术分类
减重与代谢手术的机制是通过缩小胃容积和/或缩短小肠有效长度,以达到限制摄食量和/或减少营养吸收,从而减轻体重。因此类手术同时可有效改善甚至缓解肥胖症相关疾病,包括 T2DM、NAFLD、OSAS、PCOS、高血压等且其机制独立于体重减轻,故将此类手术命名为减重与代谢手术。
按照机制可分为三类手术方式:
①以限制摄食量为主,包括:胃袖状切除术(sleeve gastrectomy,SG)和胃内球囊技术(intragastric balloons,IGB)等;
②以减少营养吸收为主,包括:单吻合口十二指肠回肠旁路联合胃袖状切除术/单吻合口十二指肠转位术(single anastomosisduodeno-ileal bypass with sleeve gastrectomy/one anastomosisduodenal switch,SADI-S/OADS)和胆胰转流并十二指肠转位术(biliopancreatic diversion with duodenal switch,BPD-DS)通常认为旷置较长胆胰肠襻的单吻合口胃旁路术(oneanastomosis gastric bypass,OAGB)也属于此类手术;
③平衡摄食量限制和营养吸收减少,包括 Roux-en-Y 胃旁路术(Roux-en-Y gastric bypass,RYGB)。
2. 手术适应证
基于高级别临床证据,综合国际肥胖和代谢病外科联盟(international federation for the surgery of obesity andmetabolic disorders,IFso)与美国代谢与减重外科学会(American society for metabolic and bariatric surgery,ASMBS)联合发布的亚洲人群减重与代谢手术的适应证,以及国内相关临床指南、专家共识,推荐手术适应证如下:
①18~70 周岁人群 BMI ≥ 32.5 kg/m2,或者 BMI ≥ 27.5 kg/m2 合并 T2DM(无论 T2DM 内科治疗是否有效);
②18~70 周岁人群 27.5 kg/m2 ≤ BMI < 32.5 kg/m2,内科减重无效,或者合并肥胖症相关其他疾病,内科治疗无效;
③ ≥70 周岁的老年人群,可参考 18~70 周岁人群手术适应证,但同时需综合考虑合并疾病及身体机能,经多学科讨论及充分知情同意后决定;
④ < 18 周岁的儿童青少年,体重超过同龄人 95% 百分位的 140%,或者体重超过同龄人 95% 百分位的 120% 且合并肥胖症相关疾病而内科治疗无效,需综合考虑合并疾病、发育状况及对未来的影响,经多学科讨论及充分知情同意后决定;
⑤重度肥胖症患者手术后,如依然处于肥胖症状态和/或病理状态,需要持续性治疗肥胖症和(或)肥胖症相关疾病,包括非手术治疗及再次手术治疗。
⑥此外,18~70 周岁人群 25.0 kg/m2 ≤ BMI < 27.5 kg/m2,且合并 T2DM,内科强化治疗血糖控制不能达标,如进行手术治疗探索,需经伦理委员会正式批准研究方案,并充分知情同意。
3. 手术禁忌证
(1)处于妊娠期的女性;
(2)滥用药物或酒精成瘾者;
(3)患有精神疾病,精神症状未有效控制或者稳定期不足 6 个月者;
(4)智力障碍或智力不成熟,行为不能自控者;
(5)不能配合术后饮食及生活习惯的改变,依从性差者;
(6)对手术预期不符合实际者。
4. 手术方式推荐
结合临床证据以及国际、国内学术组织发布的指南共识,并结合我国肥胖症人群特点,推荐如下具有高级别临床证据支持的手术方式:SG、RYGB、OAGB、SADI-S/OADS、BPD-DS、IGB(需国家药监局正式批准的球囊器械)。
其他手术方式(包括部分「袖状胃加」术式)和内镜下治疗方式(包括胃镜下袖状胃成形术(endoscopicsleeve gastroplasty,ESG)、胃镜下胃转流支架置入等),可在医学伦理委员会审核通过后,进行临床探索。
本文图表和文字内容均整理自《肥胖症诊疗指南(2024 年版)》
首发:丁香园内分泌时间
策划:白露
投稿:wangyue5@dxy.cn
点击文末「阅读原文」即可免费查看指南原文
⬇️ ⬇️ ⬇️



暂无评论内容